
Paprasti techniniai eksperimentai yra labai naudingi atliekant vaikus, tai praleidžiant laiką kartu, įdedant įgūdžius ir mažų dizainerių suprantant pagrindus, kad kepalai, kaip ir garsiajame animaciniame filme, neauga ant medžių.
Šį kartą nusprendėme pasidaryti paprasčiausią cheminės srovės šaltinį ir pabandyti jį pritaikyti viskam, kas praktiška. Kalbant apie praktinį pritaikymą, verta prisiminti, kad vos prieš keletą kartų radijo mėgėjams, norintiems tiekti savo baterinius radijo imtuvus ir stiprintuvus, buvo pasiūlyta gaminti kelių rūšių galvaninius elementus arba baterijas nepriklausomai gamybai. Tai yra „Leklanshe“ ir „Popov“ elementai [1] p. 9 ... 18 arba švino-kalio arba dujų akumuliatoriai [1], 22–28 p. Keletas santykinai didelės srovės elementų buvo prijungti prie kaitinamosios baterijos (radijo vamzdžių kaitrinės kaitros), dešimtys mažesnių elementų - prie anodo akumuliatoriaus, kurio įtampa galėjo siekti 60–80 voltų. Baterijos buvo „šlapios“ - su skystu elektrolitu ir jas reikėjo prižiūrėti bei prižiūrėti.
Taigi galvaninė ląstelė, keli žodžiai „kaip?“ ir "kodėl?" Elektros srovė atsiranda, kai metalai sąveikauja. Tokiu atveju atsiranda skirtingas potencialo skirtumas (įtampa). Dar 1793 m. Alessandro Volta, konstruodamas galvaninį elementą (Voltos polių), nustatė tuomet žinomų metalų santykinį aktyvumą: Zn, Pb, Sn, Fe, Cu, Ag, Au. Galvaninio elemento „stipris“ pasirodė didesnis, kuo toliau buvo šios eilės metalai (įtampų eilės).

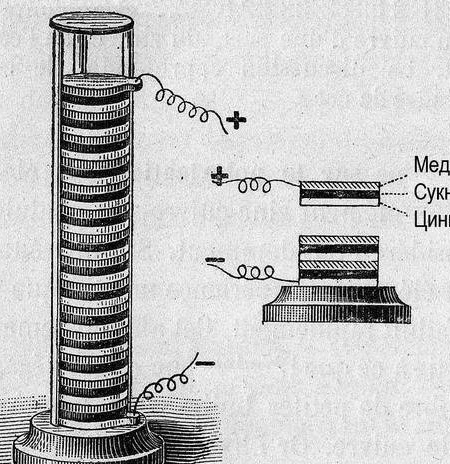
Vėliau, norint tvarkyti duomenis, „vandenilio elektrodo“ potencialas buvo laikomas nuliu. Išmatavus su juo sujungtų metalų potencialą, eksperimentiniai metalai buvo išdėstyti iš eilės. Gauta lentelė vadinosi „Elektrocheminė metalo įtempių serija“, o chemijos kabinete ji turi būti pakabinta šalia periodinės sistemos ir Dmitrijaus Ivanovičiaus portreto.
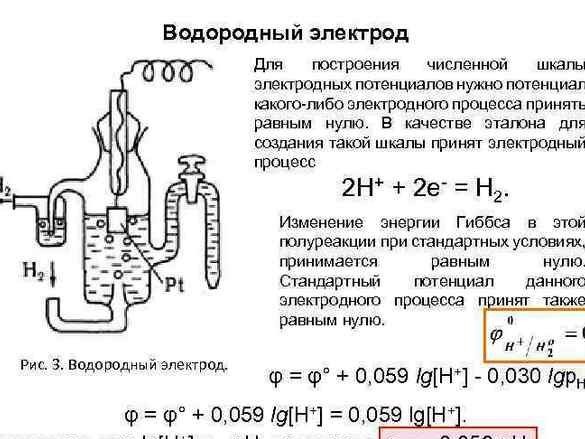

Daugybė metalo įtempių yra naudinga kontracepcija. Šiuo atveju mes, kaip ir Alessandro Volta, žinosime - kuo metalai bus atskirti vienas nuo kito, tuo didesnė įtampa bus gauta.
Savo eksperimentuose, kaip ir klasikoje, mes naudojome varį ir cinką.Kai plokštės panardinamos į elektrolitą, tarp jo ir cinko plokštės, vyksta cheminė reakcija, kurios metu plokštelėje kaupiasi neigiami krūviai ir ji yra neigiamai įkraunama. Dėl reakcijos, vykstančios galvaniniame elemente, cinko elektrodas pamažu ištirpsta.
Ant vario elektrodo, veikiant galvaniniam elementui, susidaro maži vandenilio burbuliukai, kurie izoliuoja vario paviršių nuo elektrolito. Reiškinys vadinamas, galvaninėje kameroje jis yra kenksmingas, jie su tuo kovoja. Išskiriamo vandenilio pašalinimui į elektrolitą įvedamos medžiagos, vadinamos vandeniliu. Jų vaidmenyje dažnai yra mangano junginiai, vario sulfatas. Paprastuose eksperimentuose gali būti naudojamas vaistinis kalio permanganatas.
Ką mes panaudojome eksperimentui.
Prietaisai ir medžiagos.
Galvaninių elementų, kaip varinių elektrodų, surinkimui galite naudoti vielą, vielą, foliją. Cinkas gali būti išgaunamas iš sausų elementų, gali būti naudojami cinkuoti gaminiai. Vietoj cinko galite pabandyti naudoti aliuminio ar geležies elektrodą. Natrio chloridas elektrolitui, šiek tiek minkštos tvirtinimo vielos. Jums tikrai reikia voltmetro ar multimetro, vielos pjaustytuvų, žirklių. Kaip indai gali būti naudojami tinkamo dydžio nemetaliniai indai. Stikliniai, patogesni nei lengvi plastikiniai puodeliai - jie yra sunkesni, stabilesni, sunkiau apverčiami. Labai gerai, jei yra silpnos srovės žemos įtampos apkrova - paprastas radijas, kvarcinis laikrodis ir kt.
„Aukštos įtampos“ baterija iš vielos ir varžtų.
Sužavėti detalių paprastumu ir gauta palyginti aukšta įtampa, bandėme surinkti tokią bateriją. Čia naudojama „klasikinė“ metalų pora - varis-cinkas. Idėja yra naudoti cinkuotus tvirtinimo elementus kaip cinko elektrodą. Maloniai. Akivaizdu, kad toks elementas nėra skirtas ilgalaikiam darbui - plonas cinko sluoksnis greitai ištirps, tačiau tai nėra svarbu trumpalaikiam eksperimentui. Bet cinkuoti varžtai ar krumpliaračiai visur pilna.
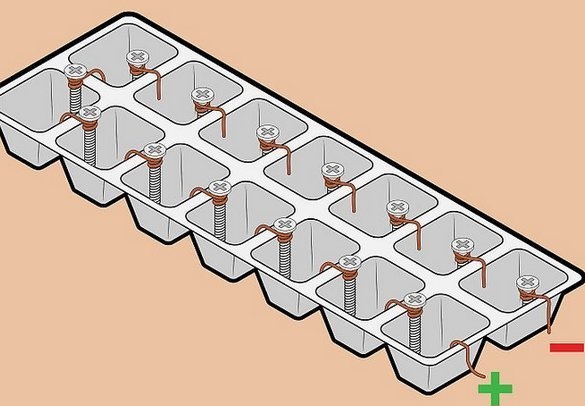
Viela taip pat naudojama kaip vario elektrodas - taip pat plačiai prieinama medžiaga, be to - patogiausias elementų montavimas akumuliatoriuje - visi elementai yra sujungti nuosekliai - plius vienas prie kito minuso. Tokiu atveju įtampa sumuojama, srovė išlieka ta pati.
Pradėkime.
Pasirinkę reikiamo ilgio cinkuotų tvirtinimo elementų skaičių, mes radome tinkamą varinę vielą. Tai apvijos viela lako izoliacijoje. Vielos skersmuo yra apie 0,5 mm.

Stulpas kelis kartus nuvalo lako izoliaciją, stengdamasis ištraukti vielą per dvigubai sulankstytą vidutinio dydžio šlifavimo šluostę.


Tada jis paruošia elektrodų porą - pagal savisriegio varžto galvutę sandariai apvynioja du ar tris vielos posūkius ir nupjauna perteklių.

Baterijos surinkimas - lovas buvo naudojamas kaip indas ledui užšaldyti. Galite naudoti dėžutes iš saldainių dėžutės, tačiau jos yra subtilesnės. Sumontavę elektrodus ant sienų tarp elementų, mes užpildome indus elektrolitu. Mes naudojome stalo druskos tirpalą - šaukštą su stikliniu 0,5 litro šilto vandens. Užpildymui labai patogu naudoti medicininį švirkštą.


Mes radome dar keletą varžtų elektrodams ir pridėjome elementų prie akumuliatoriaus - štai ką mes gavome. Įtampa esant didelėms varžoms (skaitmeninio voltmetro įėjimo varža) yra nemaža, tačiau esant bet kuriai apkrovai, kad ir kokia būtų pastebima, ji smarkiai krinta.
Pabandyk padaryti panašus galvaninis elementas (akumuliatorius) su didesniais elektrodais.
Kaip konteinerį mes naudojome pusės litro stiklainį (du), jame tilps nemažo ploto lėkštės. Kaip elektrodus mes paėmėme ploną vario foliją ir cinką - stiklo likučius iš gamyklos „sauso“ elemento, išardytą gaminant grafitą ugniai atspari danga.

Džiovintų kristalinių druskų likučius nuvalėme vieliniu šepetėliu ir apipjaustėme dviem plokštelėmis maždaug žirklėmis, kurių plotas maždaug toks pat. Iš varinės folijos iškirpkite dvi sutampančias juosteles. Taip pat su žirklėmis. Gavome dvi poras elektrodų, kurie aprūpino mūsų elementus be papildomo sujungimo, lenkdami jų kraštus ant skardinės kaklo.


Didesniame inde paruošėme elektrolitą - natrio chloridą, ištirpintą šiltame vandenyje, koncentracija vienoda, paruošti elementai pilami.


Abu elementus sujungėme nuosekliai, naudodami tvirtinimo laido gabalą ir du krokodilo spaustukus. Taigi, gerai, akumuliatoriaus įtampa yra artima standartiniam "pirštui", pabandykite naudoti. Vienas elementas, kurio įtampa 1,5 V, yra naudojamas elektromechaniniame laikrodyje, be to, dabartinis laikrodžio sunaudojimas yra labai mažas, o mūsų akumuliatorius galės jį perkrauti.

Iš laikrodžio išėmėme standartinę bateriją ir prie gnybtų prijungėme gabalą tvirtinimo laido. Stebėdami poliškumą (varinė plokštė - „+“, cinkas - „-“), savo laikrodį prijunkite prie tiesioginės eigos baterijos, voila! Laikrodis veikia, įtampa „krinta“ iki 1,3 V. Laikrodis puikiai veikė kelias valandas, kol mes visi pasigyrėme (vis dėlto burtininkas!), Tada pavargome.

Į takelį.
Bet kurio vaiko vidinė konstitucija yra tokia, kad dėmesys vienam dalykui, jis sugeba sutelkti ne daugiau kaip 15 ... 20 minučių, o visos klasės su vaikais turėtų būti suplanuotos taip, kad tuo metu jos tilptų, arba pereiti iš vienos klasės į kitą, kitaip jūs abu būsite kankinami.
Kaip apkrova, geriau tai pritaikyti, nesvarbu, ar juda, ar šviečia - voltmetro skaičiai daro įspūdį ne protui, o širdžiai. Be laikrodžių ir skaičiuotuvų, tai tikrai sukels susižavėjimą, darbas iš namų pagaminto mažo radijo imtuvo akumuliatoriaus (kaip pasirinktis - naminis!).
Ilgalaikiam naudojimui ląstelių elektrolitas turėtų būti apsaugotas nuo dulkių ir išgaravimo, taip pat pasirūpinkite depoliarizatoriumi - gerai, bent jau užkimšdami stiklainį plastikinės plėvelės gabalėliu su elastine juostele ir į elektrolitą pridėdami kalio permanganato. Be to, geriau iš karto surinkti minėtą Popovo elementą.
Be cinkuotų savisriegių sraigtų, galima naudoti cinkuotą plieno lakštą, stambesniems elementams tai yra patogiau - eksperimento metu galite gauti didelę srovę ir galią, kad ir kas būtų (pirštais judant ore).
Naudotos literatūros sąrašas.
1. P. Strelkovas. Žinok ir sugebėk. „Pioneer“ elektros inžinierius. Detgizas. 1960 metai
2. V. S. Pološinas, V. G. Prokopenko. Chemijos mokymo metodikos seminaras. Maskva, „Apšvietimas“, 1989, p. 202 203.

