Sveikinimai mūsų svetainės gyventojų!
Kasmet naftos gamyba tampa vis sudėtingesnė, o iš jos gaunamas kuras tampa vis brangesnis. ES šalyse jie paprastai grasina nustoti gaminti benzininius variklius, nori pakeisti visas transporto priemones elektriniais automobiliais. Tačiau ličio akumuliatoriai vis dar toli gražu nėra idealūs, beje, jie visai neskuba tapti idealiais. Geriausiu atveju, vienkartiniu ličio akumuliatoriaus įkrovimu bus galima įveikti ne daugiau kaip 700 km atstumą, po kurio akumuliatorių turėsite krauti maždaug savaitę, o jei įkrovimui naudosite įprastą lizdą, paprastai tai užima daug laiko. Ir jūs tik įsivaizduojate, kas nutiks, jei visi pradės nuolat krauti savo elektrinius automobilius, kokios didžiulės apkrovos bus elektros tinkle ir kokia įtampa nutekės. Apskritai ličio baterijų ateitis vis dar yra gana miglota ir kiekvienais metais vis daugiau tyrimų skiriama naujų akumuliatorių variantų paieškai.
Kaip žinote, daugiausiai energijos reikalaujantis metalas yra aliuminis. Jau mūsų laikais su kai kuriais aliuminio akumuliatorių prototipais galima nuvažiuoti apie 2000 km be įkrovimo, o tokio tipo akumuliatorių įkrovimas užtrunka tik 15 minučių, po to galima nuvažiuoti dar maždaug 2000 km.
Įkraunamos aliuminio baterijos skiriasi nuo ličio baterijų įkrovimo. Nepaisant to, jame nėra nieko sudėtingo, tereikia įkišti naują aliuminį, išpilti elektrolitą ir supilti naują elektrolitą, viskas iš esmės sutampa su benzinu mašina, tik tai yra elektrinis automobilis, o elektros tinkle nėra jokių apkrovų. Be to, norint įkrauti visus šiuos elektrinius automobilius, nereikia gaminti daugybės išparduotuvių su laidais su didžiuliu skerspjūviu.
Tačiau ne viskas čia taip sklandžiai. Iš aliuminio gauti elektrą nėra taip paprasta, kaip norėtume. Pirmiausia išsiaiškinkime, koks yra aliuminio-oro akumuliatoriaus principas.
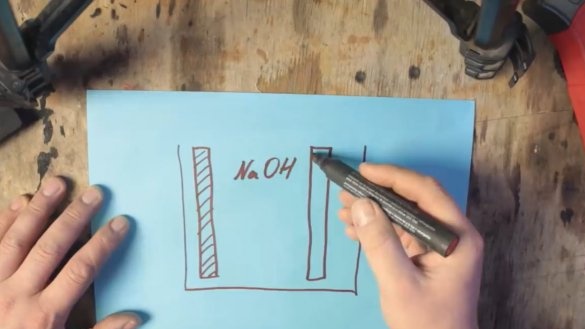
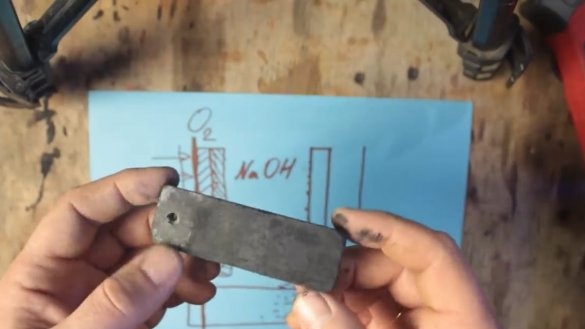
Kad tokia baterija pradėtų veikti, reikalingi 2 elektrodai: vienas natūraliai iš aliuminio, o antrasis - iš grafito. Abu šie elektrodai yra elektrolito tirpale.
Druska (NaCl) gali būti naudojama kaip elektrolitas, tačiau kartu su ja galite padidinti įtampą iki maždaug 0,7 V. Šarminio elektrolito (NaOH) įtampą galima padidinti dar daugiau - iki maždaug 1 V.
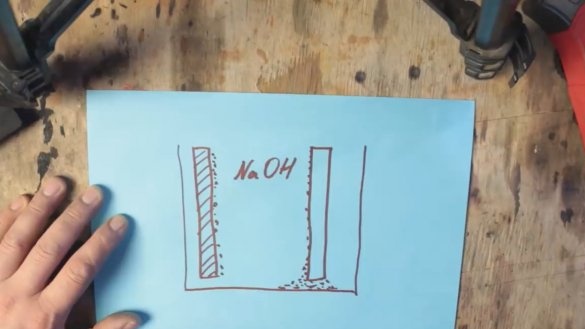
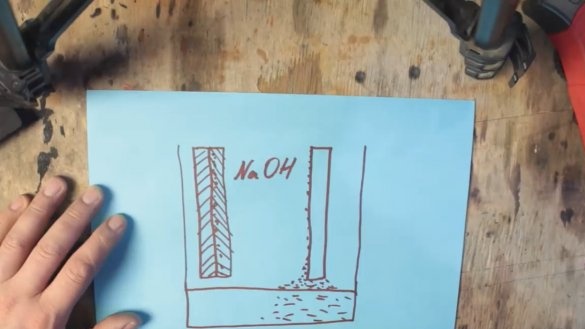
Cheminės reakcijos metu aliuminis yra padengtas aliuminio hidroksido (Al (OH) 3) sluoksniu, kuris palaipsniui grimzta į rezervuaro dugną. Ir ant grafito elektrodo paviršiaus susidaro vandenilio burbuliukai, kurie, savo ruožtu, padidina atsparumą ir sumažėja įtampa, šis procesas vadinamas poliarizacija.
Pirmąją aliuminio hidroksido kritulių problemą galima pašalinti tiesiog padidinant panaudoto produkto talpą, tačiau antrą problemą gali padėti pašalinti depoliarizuojanti masė, pagrįsta mangano oksidu, kuri eksploatacijos metu virsta mangano hidroksidu.
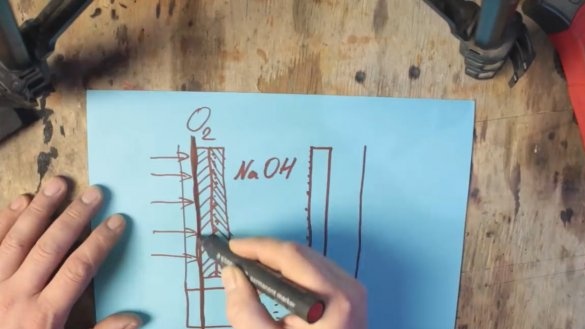
Tiesą sakant, mes gavome paprastą šarminę bateriją, bet tik labai didelę. Tačiau iškyla nauja problema. Faktas yra tas, kad taip pat sunaudojamas mangano oksidas, ir jis taip pat turės būti pakeistas. Ir mes turime užtikrinti, kad būtų naudojamas tik aliuminis. Norėdami tai padaryti, pasiimkite deguonį iš aplinkinio oro. Čia prasideda aliuminio-oro baterija. Vieną iš sienų tiesiog reikia pakeisti dujoms pralaidžia membrana, o grafito elektrodą reikia pakeisti grafito ir mangano oksido mišiniu su platinos ar sidabro nanodalelėmis.
Mangano oksidas su tauriųjų metalų nanodalelėmis nereaguoja, o veikia kaip katalizatorius, dėl kurio ore esantis vandenilis iš elektrolito oksiduojasi.
Mangano oksido su sidabro nanodalelių įtraukimu gamybos technologija iš esmės nėra sudėtinga ir gali būti išbandyta amatininkystės sąlygomis. Tačiau šiame straipsnyje aptarsime, kaip padaryti kuo taupesnį akumuliatoriaus, gaunančio energiją iš aliuminio, variantą. Šios instrukcijos yra paimtos iš „Fiery TV“ kanalo „YouTube“. Daugiau informacijos originaliame autoriaus vaizdo įraše:
Maksimali biudžetinė grafito versija yra vasariniai kontaktiniai įdėklai troleibusams. Juos galima rasti visiškai nemokamai galutinėse troleibusų stotelėse arba galite juos nusipirkti, jie nėra brangūs, autorius juos rado parduodamų po 22 rublius už vienetą.
Kitas, mums reikia šarmo. Vamzdžių valymo įrankis, kurio sudėtyje yra šimtas procentų natrio šarmų.
Norėdami pradėti šarminę reakciją, mums reikia šiek tiek, užteks 1 g šarmo 0,5 l vandens.
Pirmiausia patikrinkime, ar šioje baterijoje tikrai reikalingas grafito elektrodas. Norėdami gauti patirties, paimkime šį nerūdijančio plieno elektrodą.
Dabar mes įdėjome aliuminio plokštę ir nerūdijančio plieno elektrodą į šarmą, prijunkite multimetrą ir pažiūrėkite, kiek voltų jis pasirodo.
Kaip matai, pasirodė apie 1.4V. Dabar patikrinkime trumpojo jungimo srovę.
Trumpojo jungimo srovė pasirodė maždaug 20 mA. Kokias išvadas galima padaryti: teoriškai ekstremaliomis sąlygomis galima surinkti akumuliatorių iš nerūdijančio plieno puodelių ir aliuminio folijos.
Kitas mes turėsime vario elektrodą, pagamintą iš elektrinio vario.
Kaip galime pastebėti, įtampa pasirodė šiek tiek didesnė nei 1,4 V, tačiau trumpojo jungimo srovė iš pradžių buvo didelė, tačiau tada ji gana greitai pradėjo mažėti, o varis taip pat pradėjo būti padengtas tamsiąja danga, greičiausiai šį poveikį sukėlė priemaišos vandenyje, nes Šiame eksperimente autorius paėmė iš čiaupo.
Dabar panardinkite grafito elektrodą į elektrolito tirpalą.
Su šiuo elektrodu buvo gauta 1,3 V įtampa, trumpojo jungimo srovė sustojo maždaug 17 mA. Iš pirmo žvilgsnio atrodo, kad nerūdijančio plieno elektrodas yra efektyvesnis, tačiau nerūdijančio elektrodo paviršiaus plotas yra didesnis, todėl dar nežinoma, kuris grafitas ar nerūdijantis plienas yra geresnis.
Kadangi grafitas turi gana didelį pasipriešinimą, reikia kažkaip su tuo susitvarkyti. Būtina gaminti elektrodus iš gerai laidžios medžiagos, o grafitas turėtų būti tik jo paviršiuje.Buvo nuspręsta gręžti per grafitą, o susidariusiose skylėse supjaustyti sriegį varžtams „m6“.
Rezultatas - plieninis elektrodas su grafito apvalkalu.
Negręžto grafito varža yra apie 4,5 omo, bet gręžto grafito varža yra apie 1,7 omo.
Veide padidės atsparumas ir atitinkamai padidės struktūros efektyvumas. Tolesniuose eksperimentuose naudosime distiliuotą vandenį.
Pirmasis eksperimentas su elektrolitu, kuriame 1 g vandens yra 4 g šarmo.
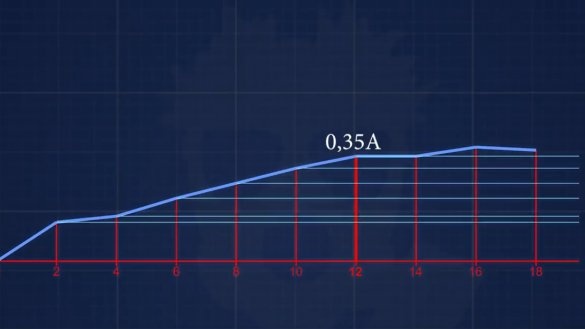
Trumpojo jungimo srovė pasirodė 150mA. Kitame elektrolite yra 6 g šarmo 1 litre. Na ir taip toliau, kiekvieną kartą padidinsime koncentraciją 2 g, kol pasieksime tokią koncentraciją, kurioje srovė nedidės.
Nors tokia paprasta baterija neturi didelio srovės efektyvumo, tačiau tokia baterija gali veikti labai ilgą laiką, o elektrodai gali būti naudojami bet kokie aliuminiai, kuriuos lengvai galima išlydyti į bet kokios formos elektrodus, pavyzdžiui, aliuminio skardines. įvairūs alkoholiniai ir nealkoholiniai gėrimai, šokolado folija ir kt.
Dėl to, atlikus visus eksperimentus su skirtingomis elektrolito koncentracijomis, tampa aišku, kad esant tokiai akumuliatoriaus konstrukcijai nėra prasmės į 1 litrą vandens pilti daugiau kaip 12 g šarmo, tai yra, mes gauname apie 1% tirpalo.
Tada autorius surinko dar vieną spaustuką, susidedantį iš 3 elektrodų.
Dvi baterijos suteikia aukštesnę įtampą ir mažiau nuostolių, todėl rezultatas bus geresnis.
Dabar paimkime kibirą elektrolito, didelį aliuminio gabalą ir 2 nerūdijančio plieno elektrodus.
Kibire elektrolito koncentracija 10g / 1l. Didžiausia srovė 1,3A, ji sumažėjo iki 520mA. Su visu didžiuliu nerūdijančio plieno plotu jis nebuvo lyginamas su grafitu, nes pasirodė, kad jis su grafitu buvo 600 mA. Beje, reakcijos metu išsiskiria vandenilis, kurį taip pat galima surinkti ir panaudoti kaip energijos šaltinį. Žodžiu, yra kur augti. Tai viskas kol kas. Ačiū už dėmesį. Greitai pasimatysime!